Madame R., 100 ans, est adressée dans le service pour une désaturation fébrile associée à une toux grasse.
• Autonome au domicile
• Marche avec un déambulateur
• Hypertendue et dyslipidémique
• Vaccinée contre le Covid-19 avec le Johnson & Johnson en juin 2021
À l’examen clinique, il existe des crépitants bilatéraux. Le bilan biologique retrouve un syndrome inflammatoire avec une CRP à 93 mg/l et des polynucléaires neutrophiles à 9 G/l ; les D-Dimères sont augmentés à 1 800 µg/l. Les gaz du sang en air ambiant retrouvent une hypoxémie isolée avec une pO2 à 64 mmHg.
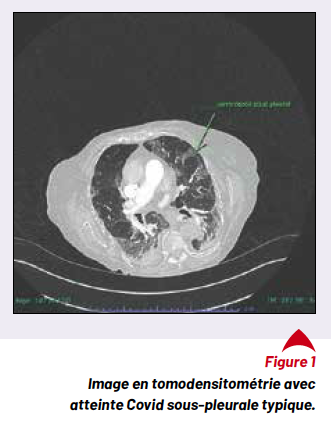
L’angioscanner thoracique ne met pas en évidence d’embolie pulmonaire, mais la présence de foyers alvéolo-interstitiels de siège postéro-basal bilatéral en verre dépoli. La PCR SARS-CoV-2 est positive.
Le diagnostic de pneumopathie Covid hypoxémiante est alors posé et un traitement par dexaméthasone est débuté, en parallèle d’une anticoagulation préventive et de la mise sous O2 aux lunettes à 3 l/min.
En raison de la majoration des besoins en oxygène, une discussion collégiale entre réanimateurs et gériatres est faite. Il est décidé de ne pas admettre la patiente en réanimation, compte tenu de son âge et ses comorbidités, et des risques inhérents à une intubation invasive. Les ressources techniques et humaines du CH Alès-Cévennes permettent alors la mise en place d’oxygénation à haut débit (OHD) en service de court séjour gériatrique.
L’amélioration clinique commence au bout d’une dizaine de jours permettant le sevrage progressif jusqu’au retour à l’oxygénation aux lunettes nasales, et la poursuite de la prise en charge dans un service de soin et de réadaptation avant son retour à domicile.
Principes de l’oxygénothérapie à haut débit par lunettes nasales (OHD)
L’OHD est une technique utilisée au départ en néonatalogie dans les années 2000 pour assister les enfants en détresse respiratoire au cours des bronchiolites. Chez l’adulte, la technique s’est développée depuis 2004 du fait des contraintes techniques liées à la nécessité de débits plus élevés. En effet, contrairement aux nourrissons, les adultes ne sont pas « respirateur nasal obligé ».
Le principe de l’OHD est fondé sur deux principes, l’oxygénation et l’humidification, mais de nombreux autres avantages physiopathologiques sont attendus (baisse du travail respiratoire, recrutement alvéolaire) [1].
L’oxygénation
Il s’agit de fournir au patient un mélange air/oxygène de FiO2 fixe (fraction inhalée d’oxygène = pourcentage d’oxygène contenu dans le mélange inspiré) et connu à un débit suffisamment élevé pour couvrir le débit inspiratoire maximal instantané. Cela permet de rendre la FiO2 stable, indépendante de la fréquence respiratoire, du volume courant, et du mode ventilatoire du patient. Les méthodes traditionnelles d’oxygénothérapie ne permettent pas d’assurer une FiO2 fixe (ni même suffisamment élevée lorsqu’on se situe dans les tranches de FiO2 > 80 %). Le haut débit permet aussi de maintenir la FiO2 que ce soit bouche fermée ou ouverte [1].
L’humidification [1]
L’inhalation de gaz non humidifié est toxique pour les voies respiratoires et entraîne une abrasion de la muqueuse bronchique, une diminution de la clairance mucociliaire et une altération du surfactant.
L’humidification de l’air inspiré et son réchauffement sont physiologiquement assurés par les voies respiratoires. Ainsi, en cas de demande ventilatoire augmentée les capacités d’humidification peuvent être dépassées et déclencher un bronchospasme, comme en atteste l’augmentation de l’incidence de l’asthme d’effort lors des sports de glace.
Compte tenu des débits nécessaires au cours d’un traitement par OHD, le réchauffement et l’humidification des gaz inspirés sont d’autant plus indispensables. Cette humidification a probablement un grand rôle dans les résultats thérapeutiques de cette technique, comme cela peut se voir pour l’amélioration de l’asthme d’effort dans une ambiance humide et réchauffée.
L’étude FLORALI a propulsé l’OHD en traitement de première ligne des détresses respiratoires hypoxémiques [2]. En effet, elle diminue le taux d’intubation et améliore la survie des patients avec des critères de sévérité (PaO2/FiO2 inférieur à 200) par rapport à l’oxygénothérapie standard et la ventilation non invasive (VNI). Si les rôles de l’humidification et de la maîtrise optimale de l’oxygénation peuvent suffire à expliquer l’effet favorable de la technique, les gains en amélioration des signes de détresse et de dyspnée sont l’expression de son effet sur le travail respiratoire.
L’OHD a progressivement été proposée dans toutes les formes d’insuffisances respiratoires aiguës (IRA) hypoxémiques :
• pneumonies,
• œdème aigu du poumon,
• embolie pulmonaire,
• poussées d’hypertension artérielle pulmonaire (HTAP),
• gestes invasifs chez des hypoxémiques,
• certains cas de décompensations de BPCO,
• dans la pré-oxygénation avant une intubation
• et en anesthésie.
En ce qui concerne l’utilisation de l’OHD pour des patients Covid, de nombreuses séries italiennes, dictées par la rapide saturation des unités de réanimations, ont entraîné son utilisation en service conventionnel, moyennant formation et incrément dans la surveillance [3-5].
Pour certains patients ayant des troubles du comportement entraînant un refus ou une mauvaise compliance à la VNI, l’OHD peut être une solution intermédiaire à ne pas négliger. Elle peut aussi se révéler intéressante dans le contexte de soins palliatifs, compte tenu de l’amélioration sur la dyspnée et le confort respiratoire [1].
Fiche technique OHD [1] (Fig. 2 et 3)
Avantages/inconvénients/freins
Avantages
L’avantage majeur de la technique est sa relative simplicité d’utilisation, puisque par rapport à la VNI, nul besoin de régler trigger, PEP, niveau de pression inspiratoire, cyclage, asynchronies, etc.
Effets secondaires [1]
Il a été décrit d’exceptionnels fistules bronchopleurales, pneumomédiastin et pneumothorax.
Inconvénients/risques
Deux risques majeurs se dessinent. D’une part, la facilité d’utilisation risque de retarder une intubation nécessaire, à l’instar de ce qui est observé avec la VNI. Cela peut grever le pronostic du patient. D’autre part, le risque pour les patients avec insuffisance respiratoire hypercapnique pour lesquels l’OHD ne peut se substituer à la VNI ou à la ventilation mécanique en cas d’acidose respiratoire. L’OHD doit être, dans ce contexte, réservée aux échecs de VNI ou à l’oxygénothérapie entre les séances de ventilation.
Surveillance
La surveillance d’un patient sous OHD est celle de tout patient en détresse respiratoire aiguë : fréquence respiratoire, SpO2, état de conscience, fièvre, hémodynamique…
En permettant de connaître la FiO2 administrée, l’OHD permet de calculer le rapport PaO2/FiO2 qui est le critère international pour classifier la gravité d’une IRA. L’évolutivité de ce rapport, dans le sens d’une augmentation ou d’une diminution, signe une amélioration ou une aggravation du patient. Le « ROX
index » reposant sur le rapport SpO2/FiO2 associé à la clinique (fréquence respiratoire) a fait preuve de sa validité pour l’OHD, et permet une estimation globale de sa tolérance et de l’évolution du patient.
Freins
Il y a eu de nombreuses craintes à voir l’OHD quitter la sphère de la réanimation de par des contraintes structurelles (quantité d’oxygène disponible sur les réseaux, nombre d’appareils), humaines (surveillance des patients, formation des équipes), mais aussi psychologiques – car l’OHD s’adresse à des patients en défaillance vitale qui peuvent déstabiliser des équipes. Les médecins et réanimateurs étaient aussi parfois réticents compte tenu du profil des malades auxquels elle s’adresse et du risque inhérent d’intubation trop tardive.
La pandémie de Covid, et la contrainte de soigner les patients qui en étaient atteints en détresse respiratoire aiguë (DRA) en dehors des services de réanimation saturés, a permis la popularisation de l’OHD et ainsi la possibilité d’achat d’appareils pour certains centres.
Malgré sa simplicité d’utilisation, une formation du personnel est bien sûr nécessaire pour la maîtrise des indications et de la technique sans perte de chance pour les patients. En revanche, il existe une grande hétérogénéité dans la surveillance continue allant de la centrale d’alarme, comme en soins continus, à un relevé des constantes au mieux toutes les 6 h pour ce qui concerne les unités d’hospitalisation standard. Le problème n’est pas tant les paramètres à relever que la fréquence de visite. Ainsi, selon le niveau d’engagement thérapeutique, le « cut off », du ROX doit être révisé et adapté à la structure de soin dans laquelle se trouve le patient, afin de dégager des marges de sécurité [4].
L’OHD en gériatrie
Prise en charge hors soins intensifs
Au-delà de la problématique de l’OHD en gériatrie, se dégage celle de l’OHD hors les murs des unités de médecine intensive. Les patients non admis en réanimation, ou ceux pour lesquels des décisions de limitation de traitements ont été prises, doivent pouvoir disposer des conditions disponibles à l’hôpital afin que leur prise en charge, palliative ou non, puisse assurer le confort du patient et un accompagnement des familles.
Réévaluation
La réévaluation est particulièrement nécessaire chez les patients les plus graves et les plus fragiles pour lesquels la décision initiale se fait dans un contexte d’incertitude avec le concept de réanimation d’attente (c’est-à-dire « faire et réévaluer » plutôt que « ne pas faire »).
Dans toutes les situations de décisions d’orientation, y compris en dehors de la pandémie, les patients, leurs proches et l’ensemble des personnels soignants doivent être informés du caractère extraordinaire, mais personnalisé, des mesures mises en place.
Il ne faut pas que la population gériatrique ou fragile fasse les frais de circonstances dites exceptionnelles en devenant les premières “victimes” des « Do Not Intubate Order ». Certains patients ayant été récusés de soins d’intubation doivent malgré tout pouvoir bénéficier du maximum des thérapeutiques disponibles hors intubation et constituent la population des « curatifs limités ». De fait, en situation de tension hospitalière, pour permettre d’offrir aux patients un traitement tel que l’OHD il nous faut distinguer au minimum trois catégories de patients :
1- Le patient dont l’indication n’est liée qu’au confort dans une situation palliative pure. Dans ce cas point besoin de ROX, la surveillance d’un score de dyspnée et/ou de confort quel qu’il soit, en fonction des protocoles locaux, est suffisant.
2- Le patient accueilli en service de médecine conventionnelle par saturation des unités de médecines intensives. Il nécessite une surveillance rapprochée par du personnel formé, au mieux en continu si l’environnement technique le permet. Certains centres ont équipé des chambres avec un monitoring relié à une centrale située en salle de soins [4, 5]. L’alerte de dégradation fondée sur un seuil de ROX modifié (niveau d’alerte de + 1 point) [4, 5] permet au réanimateur en pré-alerte d’intervenir précocement. Le ratio patient/personnel soignant (médical et paramédical), les modalités de permanence de soins, la formation et l’environnement technique sont les principales limites rencontrées. La littérature concernant ce problème ne permet pas de trancher sur la perte de chance ainsi liée à cette nécessité d’accueil par défaut.
3- Le patient pour lequel on pourrait développer la notion de « curatif limité » (« do not intubate » des Anglo-Saxons) auquel on octroie toutes ses chances hors de l’intubation. Dans ce cas de figure, reste à savoir si les moyens de surveillance influent sur le pronostic entre les unités de médecine intensive et les unités d’hospitalisation standard. Le peu de littérature disponible ne permet pas de trancher. Le taux d’échec défini comme l’admission en unité de médecine intensive ou le décès oscillant selon les études entre 35 et 83 % [3-7].
Conclusion
La question de l’engagement thérapeutique en gériatrie est donc constante dans nos pratiques, avec limitation d’une ou plusieurs thérapeutiques, et le non-accès à des unités de soins intensifs ou de réanimation. Au final, l’irruption de l’OHD, technique dite de “réanimation”, dans les soins quotidiens pose des questions et les réponses sont multifactorielles. Les diverses expériences rapportées ne sont nullement comparables. Le point positif est que la technique a diffusé et qu’il va rester à la communauté médicale de se l’approprier. Compte tenu de l’évolution démographique, une réflexion doit être effectuée dans les services d’urgence, de réanimation et de gériatrie sur l’évaluation et la prise en charge optimale des patients âgés. La création d’USI gériatriques dédiées dans les services de gériatrie avec les moyens humains et techniques peut être une des solutions.
Les auteurs déclarent ne pas avoir de lien d’intérêt.
Bibliographie
1. Nishimura M, High-Flow Nasal Cannula Oxygen Therapy in Adults: Physiological Benefits, Indication, Clinical Benefits, and Adverse Effects. Respiratory care 2016 ; 61 : 529-41.
2. Frat JP, Thille AW, Mercat A et al., High-fow oxygen through nasal cannula in acute hypoxemic respiratory failure. N Engl J Med 2015 ; 372 : 2185–96.
3. Zemach S, Helviz Y, Shitrit M et al., The Use of High-Flow Nasal Cannula Oxygen Outside the ICULevin. Respiratory care 2019 ; 64 : 1333-42.
4. Vega ML, Dongilli R, Olaizola et al., COVID-19 Pneumonia and ROX index: Time to set a new threshold for patients admitted outside the ICU. Pulmonology 2022 ; 28 :13-17.
5. Franco C, Facciolongo N, Tonelli R et al., Feasibility and clinical impact of out-of-ICU noninvasive respiratory support in patients with COVID-19-related pneumonia. Eur Respir J 2020 ; 56 : 2002130.
6. Hacquin A, Perret M, Manckoundia P et al., High-Flow Nasal Cannula Oxygenation in Older Patients with SARS-CoV-2-Related Acute Respiratory Failure. J Clin Med 2021 ; 10 : 3515.
7. Nadeem I, Jordon L, Rasool MU et al., Role of advanced respiratory support inacute respiratory failure in clinically frail patients with COVID-19. Future Microbiol 2022 ; 17 : 89-97.