Thrombose et cancer : quelle prise en charge chez le sujet âgé ? [1]
La thrombose associée au cancer (TAC) est la conséquence de la coexistence de quatre dimensions majeures (Fig. 1) :
• les facteurs liés au patient,
• les facteurs liés à son cancer,
• les facteurs liés au traitement de son cancer
• et les conditions liées à l’inflammation.

Figure 1 – Les quatre dimensions de la TAC.
Prévention primaire des événements thrombotiques
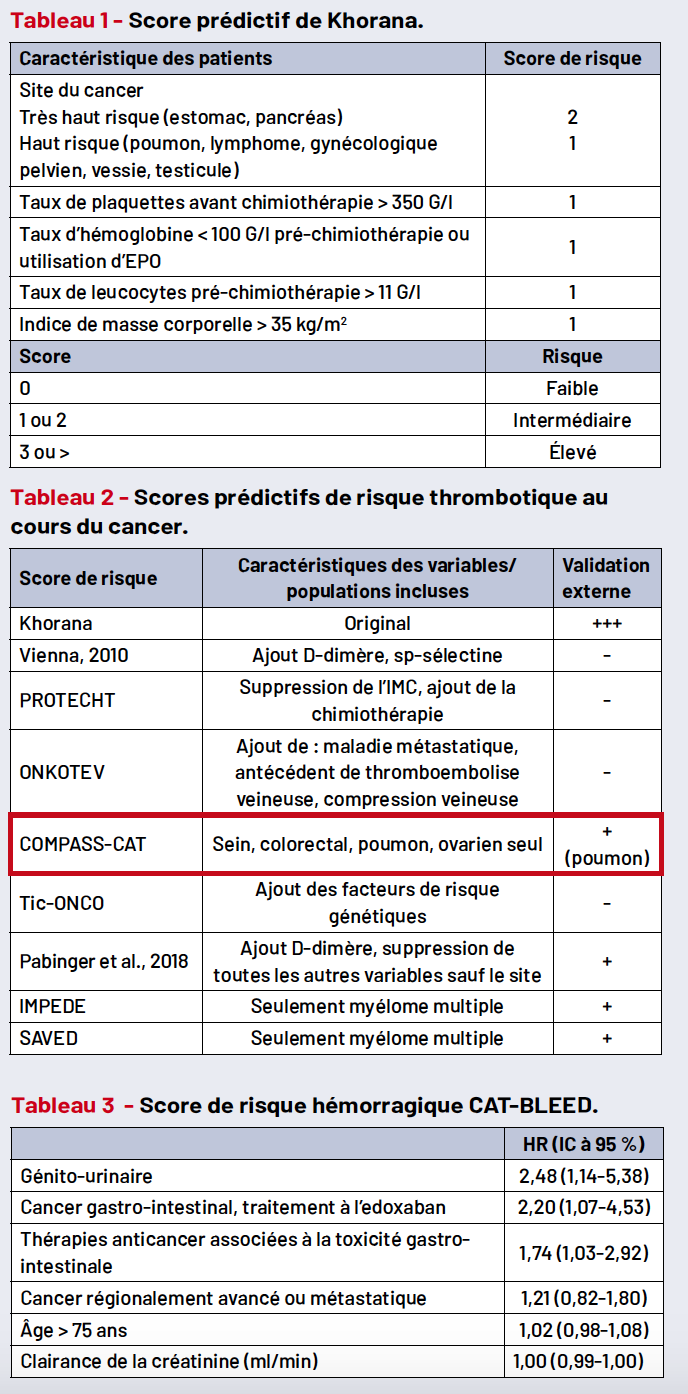
Avant la chimiothérapie, l’un des premiers scores d’évaluation du risque de maladie thromboembolique veineuse (MTEV), et donc de thrombose, chez un patient présentant un cancer est le score de Khorana (Tab. 1). Le risque selon le score est classifié comme faible (score = 0), intermédiaire (score = 1 ou 2) et élevé (score ≥ 3).
Aujourd’hui, des données solides indiquent l’évaluation d’un risque élevé avec un score ≥ 2.
Au cours du cancer, le risque thrombotique augmente et il faut donc le réévaluer. Cependant, le score de Khorana n’a pas été validé pour évaluation du risque pendant ou après la chimiothérapie. Ainsi, concernant la prédiction du risque thromboembolique chez ces patients, on utilisera les scores répertoriés en tableau 2.
La complexité de la gestion du risque de thrombose chez le patient cancéreux réside également dans la maîtrise du risque hémorragique, aggravé par les anticoagulants. Toutefois, les scores de risque de saignement existants (ACCP-VTE, HAS-BLED, RIETE, VTE-BLEED…) chez les patients atteints de la MTEV ne sont pas performants chez les patients atteints de TAC. Le score CAT-BLEED (Tab. 3) semblera donc mieux pour évaluer le risque hémorragique dans cette population. De plus, le type de cancer ainsi que d’autres facteurs de risque bien établis, comme antécédents de saignement, thrombocytopénie sévère ou anémie, doivent être pris en compte pour évaluer le risque hémorragique avant la prescription d’une thromboprophylaxie.
Traitement personnalisé des événements thrombotiques
Les dernières préconisations de l’AFSOS (Association francophone des soins oncologiques de support), validées en juillet 2021, proposent un arbre décisionnel de thrombo-prophylaxie chez le patient cancéreux (www.afsos.org/wp-content/uploads/2018/12/Prise-en-charge-de-la-maladie-thromboembolique-veineuse-en-cancérologie_2021.pdf) (Fig. 2).

Figure 2 – Préconisation AFSOS pour la prévention primaire de la MTEV.
Anticoagulants
Le choix de l’anticoagulant devra être évalué en fonction des interactions médicamenteuses, du site du cancer et des facteurs de risque liés au patient, sa vulnérabilité et ses comorbidités.
Par exemple, les inhibiteurs de PGP (P-glycoprotéine) et/ou de cytochrome (CYP P450) augmentent le risque hémorragique, tandis que les inducteurs de PGP et de CYP P450 augmentent le risque thrombotique.
Pour les héparines bas poids moléculaire (HBPM), il n’a pas été observé d’interaction avec les traitements anticancéreux.
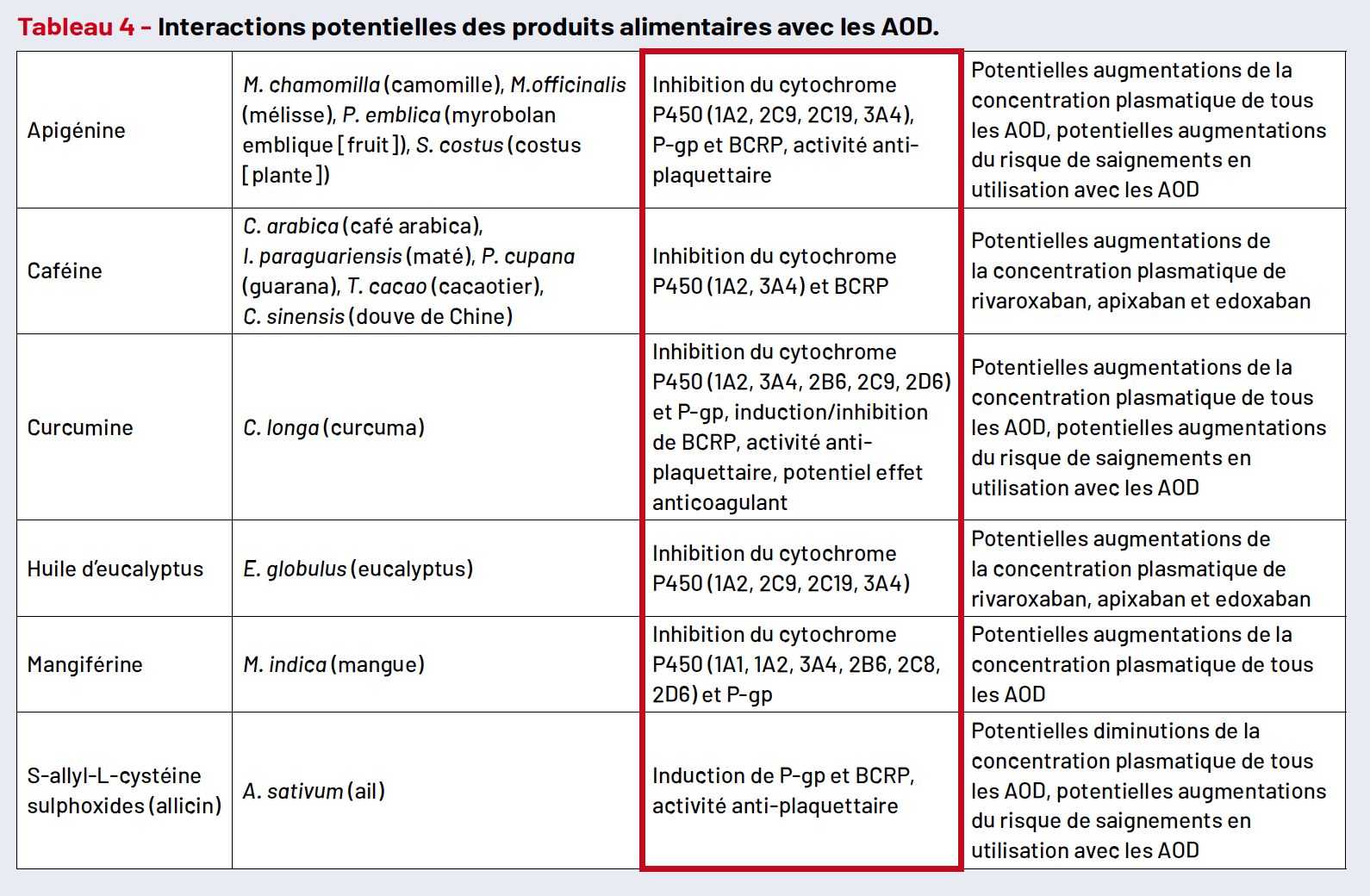
En revanche, la situation est plus complexe avec les anticoagulants oraux directs (AOD) dont la mise en place nécessite une évaluation personnalisée. En effet, l’interaction médicamenteuse avec les AOD est importante chez les patients cancéreux adeptes de la médecine douce, comme le suggère un article récent ayant recensé plus de 250 interférences potentielles [2], par exemple avec la camomille, le café, le curcuma, l’eucalyptus, la mangue, ou même l’ail pouvant potentialiser ou inhiber l’effet anticoagulant des AOD (Tab. 4).
Traitement anticoagulant pendant les 6 premiers mois
Dans les recommandations de bonne pratique pour la prise en charge de la maladie veineuse thromboembolique chez l’adulte, Sanchez et al. [3] préconisent de :
• traiter les malades atteints de cancer actif et d’une thrombose veineuse proximale ou d’une embolie pulmonaire par HBPM sans relais par anti-vitamine K (AVK) pendant les 6 premiers mois de traitement ;
• prescrire un AOD plutôt qu’un AVK en cas d’intolérance aux HBPM, quand le risque hémorragique est faible, sauf cancer digestif ou urologique.
Traitement anticoagulant après les 6 premiers mois
Après 6 mois de traitement anticoagulant pour un événement thromboembolique veineux (ETEV) dans un contexte de cancer, il est recommandé de :
• poursuivre le traitement anticoagulant lorsque le cancer est actif (présence d’une maladie tumorale détectable, y compris par l’existence d’un biomarqueur, et poursuite d’un traitement anti-tumoral, y compris l’hormonothérapie, dans les 6 mois),
• renouveler l’indication du traitement anticoagulant tous les 6 mois en cas de poursuite du traitement après une récidive thromboembolique pendant les 6 premiers mois de traitement.
Traitement des récidives thromboemboliques veineuses sous traitement anticoagulant
Devant une récidive thromboembolique sous :
• traitement par AVK, il est suggéré de remplacer l’AVK par une HBPM à dose curative,
• traitement par HBPM, si la dose d’HBPM est inférieure à la dose curative, il est suggéré de revenir à une posologie curative et d’augmenter la dose d’HBPM de 25 % si l’HBPM était déjà donnée à dose curative.
Il est également suggéré de ne pas utiliser de filtre cave en cas de récidive de MTEV sauf si la récidive est une embolie pulmonaire grave et/ou que le risque hémorragique est élevé ne permettant pas d’augmenter la dose d’HBPM.
Traitement des thromboses sur cathéters veineux centraux
Il est suggéré de traiter les thromboses veineuses profondes symptomatiques sur cathéter veineux central pendant au moins 3 mois, que le cathéter soit retiré ou non. Seront alors indiqués les HBPM et AVK plutôt que les AOD. Dans le cas où le cathéter est laissé en place et que le cancer est actif, le traitement anticoagulant pourra être poursuivi au-delà de 3 mois.
Traitement des embolies pulmonaires de découverte fortuite
Les embolies pulmonaires (EP) découvertes fortuitement, quel que soit le niveau anatomique, seront traitées de la même manière que les EP symptomatiques, si le diagnostic est formellement confirmé.
Traitement des thromboses veineuses superficielles
Il est recommandé de traiter de manière curative pendant au moins 3 mois et ensuite discuter la stratégie en RCP.
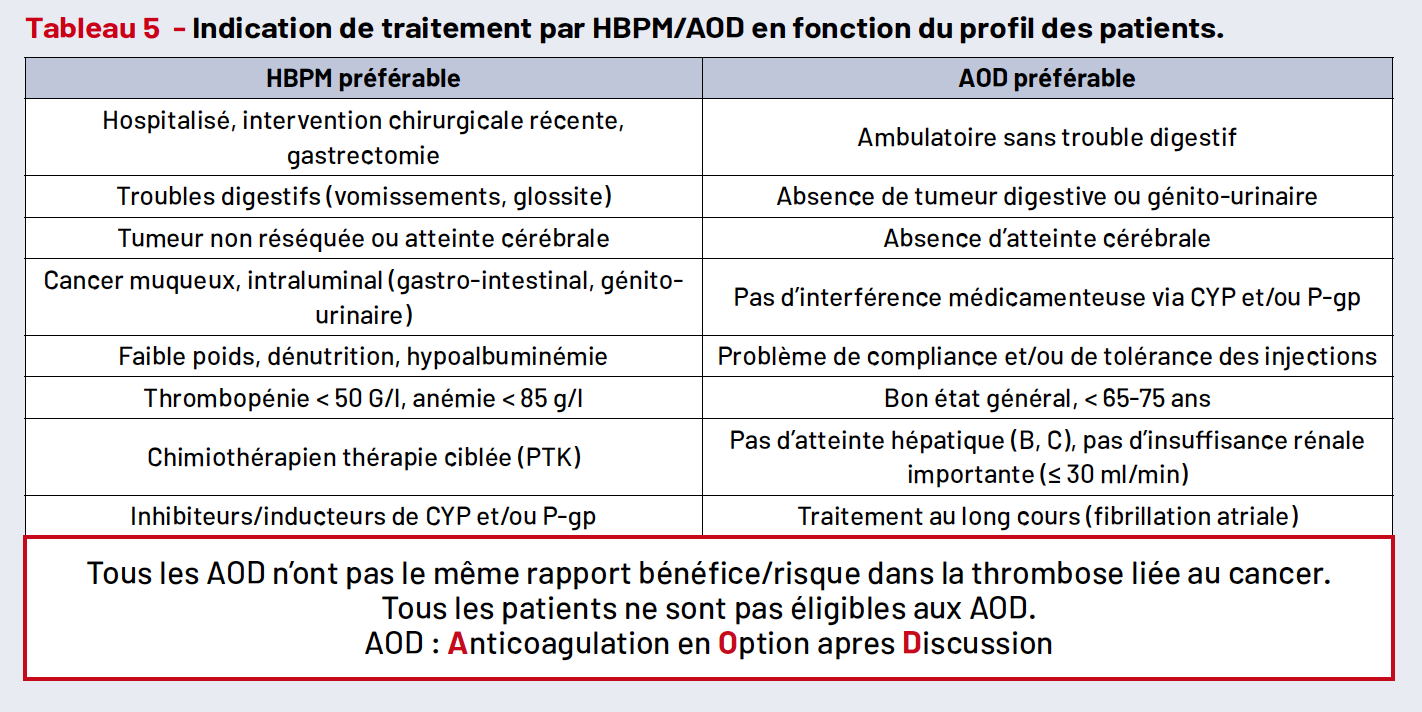
À RETENIR (Tab. 5)
• L’HBPM reste préférable dans des situations de vulnérabilité.
• Les AOD sont plus simples à utiliser et sont réservés aux patients ambulatoires avec un traitement anticoagulant prolongé.
Bibliographie
1. Elalamy I. Thrombose et cancer : quelle prise en charge chez le sujet âgé ? Journée scientifique de Broca 2021.
2. Grześk G, Rogowicz D, Wołowiec Ł et al. The Clinical Significance of Drug-Food Interactions of Direct Oral Anticoagulants. Int J Mol Sci 2021 ; 22 : 8531.
3. Sanchez O, Benhamou Y, Bertoletti L et al. Recommandations de bonne pratique pour la prise en charge de la maladie veineuse thromboembolique chez l’adulte. Rev Mal Resp 2021 ; 38 : e1-6.
Amylose : une nouvelle cause d’insuffisance cardiaque chez le sujet âgé
Sur le plan physiopathologique, l’amylose rappelle le mode opératoire du cancer au cours duquel les cellules se multiplient et envahissent les organes. Dans l’amylose, ce sont les protéines qui changent de conformation et se multiplient. C’est un processus dynamique et exponentiel. Les fibrilles infiltrent les organes dans la matrice extracellulaire, les épaississent et bloquent leur fonctionnement. Il s’agit de maladies systémiques caractérisées par l’accumulation de fibrilles amyloïdes dans différents organes tels que le cœur, le rein, le foie, le système gastro-intestinal et nerveux, provoquant ainsi l’altération structurelle et la dysfonction des organes atteints.
Dans le cas des amyloses cardiaques (AC) chez le sujet âgé (Un article détaillé ainsi qu’un cas clinique sur l’amylose cardiaque peuvent être consultés dans le N°194 de Repères en Gériatrie [2].)
, le diagnostic est primordial, surtout en présence d’insuffisance cardiaque (IC) (13 % des patients avec une IC à FEVG préservée ont une amylose à transthyrétine). De même, chez 16 % des patients ayant eu TAVI, on retrouve une amylose à transthyrétine sénile, responsable à la fois de l’hypertrophie cardiaque et de l’atteinte valvulaire.
Un patient ayant une amylose à transthyrétine (TTR) va ainsi être suivi pour cardiopathie hypertensive, sténose aortique, IC à FEVG préservée ou altérée et fibrillation atriale. Cette représentation clinique est liée à la répartition des dépôts amyloïdes dans l’ensemble du myocarde, dans l’endocarde et les valves.
Le diagnostic : quand y penser ?
Au moment du diagnostic, les patients présentent les signes cliniques regroupés sous l’acronyme EPOF (essoufflement, prise de poids, œdèmes et fatigue). Il faut rechercher, en plus, les atteintes extra-cardiaques, assez fréquentes chez les patients souffrant d’amyloses à transthyrétine. La particularité de cette maladie est que l’atteinte commence au niveau des téguments et des articulations 5 à 10 ans avant le diagnostic de l’amylose : des atteintes au niveau des canaux carpiens de manière bilatérale, des ruptures tendineuses du long biceps ou des ruptures de la coiffe des rotateurs, des canaux lombaires étroits, une surdité.
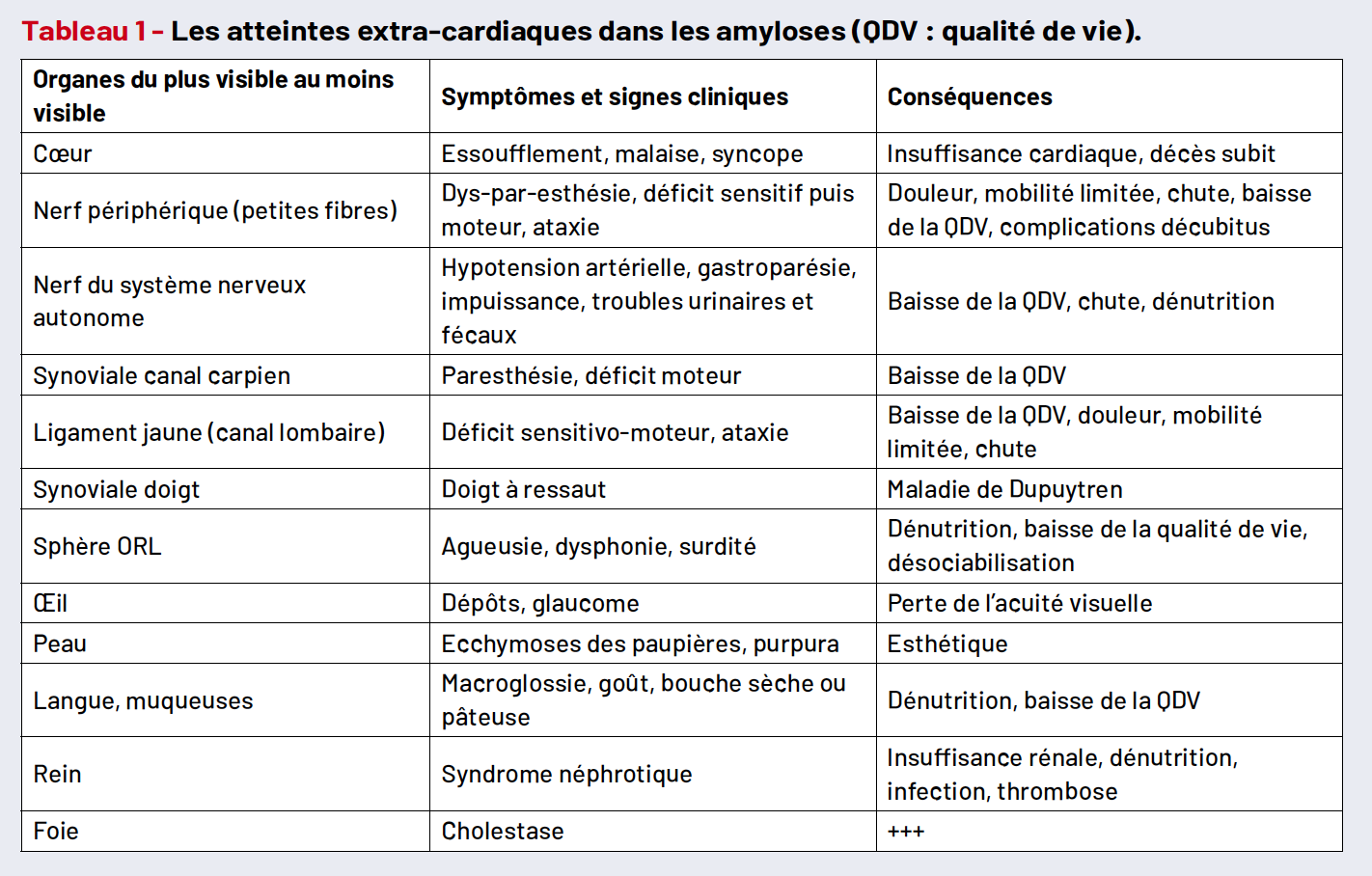
Les signes cliniques dépendent des organes touchés (Tab. 1) :
• manifestations cardiaques :
o insuffisance cardiaque à FEVG préservée avec hypertrophie ventriculaire gauche concentrique retrouvée à l’ETT,
o résistance aux traitements habituels de l’IC, avec poussées itératives,
o microvoltage paradoxal à l’ECG ;
• manifestations ostéo-articulaires :
o syndrome du canal carpien,
o syndrome de Dupuytren,
o syndrome du canal lombaire étroit,
o rupture du tendon de l’épaule et/ou biceps,
o lésions unguéales ;
• manifestations neurosensorielles :
o neuropathie des extrémités,
o macroglossie,
o dysautonomie (diarrhées, vomissements)
o et hypotension orthostatique.
Amylose et fragilité
Les gériatres sont plus que concernés par cette pathologie et la fragilité de ces patients. En effet, les conséquences des AC pour les patients âgés sont :
• autonomie : 69 % des patients en perte d’indépendance fonctionnelle,
• neuro-cognitives : 72 % de syndromes dysexécutifs,
• thymiques : 49 % de syndromes dépressifs,
• motrices : faiblesse musculaire (74 %), troubles de la marche et de l’équilibre (58 %), sédentarité (47 %), risque de chute (42 %) et sarcopénie,
• nutritionnelles : anorexie, amaigrissement (31 %), malnutrition (39 %),
• vésico-sphynctériennes : incontinence urinaire par hyperactivité vésicale,
• et asthénie (61 %).
Les tests utilisés pour l’évaluation globale et le dépistage de la fragilité dans le cadre d’une AC sont :
• le score Short Emergency Geriatric Assessment (SEGA) pour le dépistage de la fragilité (non fragile : score ≤ 8 ; fragile et très fragile : score > 8) ;
• les échelles ADL et IADL pour évaluer l’autonomie ;
• un bilan de débrouillage cognitif avec notamment Mini-Mental State Examination (MMSE) et une évaluation des fonctions exécutives (BREF et Horloge),
• évaluation de la dépression avec l’échelle Geriatric Depression Scale (GDS ou mini-GDS) ;
• évaluation de la performance physique, de l’équilibre et de la force musculaire par le Short Physical Performance Battery (SPPB) ;
• le Mini Nutritional Assessment (MNA) pour évaluer l’état nutritionnel ;
• évaluation des fonctions vésico-sphynctériennes par l’Urinary Symptom Profile (USP).
Bilans
Bilan de l’amylose
Le diagnostic de l’amylose cardiaque repose sur des examens non invasifs et le recours à un centre expert dans l’amylose cardiaque. Les examens à demander en première intention devant une suspicion d’amylose cardiaque sont :
• un bilan biologique :
o biomarqueurs : NT-proBNP et troponine ultrasensible,
o électrophorèse des protéines sériques (EPP), immunofixation et dosage des chaînes légères libres,
o recherche de protéinurie de Bence-Jones,
o bilan hépatique et rénal ;
• ECG :
o microvoltage,
o troubles conductifs,
o fibrillation auriculaire ou flutter ;
• échocardiographie :
o examen central pour évoquer le diagnostic,
o hypertrophie ventriculaire gauche circonférentielle,
o altération typique du strain (altéré à la base du VG, préservé à l’apex du VG),
o insuffiisance cardiaque à FEVG préservée ;
• IRM cardiaque : réalisation d’une biopsie cardiaque permettant de confirmer histologiquement l’amylose et, quand il y a une gammapathie, différencier l’amylose AL (immunoglobulinique) et amylose TTR.
Le bilan pourra être complété en milieu spécialisé par une scintigraphie osseuse aux biphosphonates (notamment pour les amyloses à transthyrétine [2]).
Prise en charge de l’amylose
Elle se fait en collaboration avec les services de référence des maladies rares spécialisés dans l’amylose. En effet, l’expérience a montré que les guidelines de l’insuffisance cardiaque chez les patients souffrant de l’amylose ne doivent pas être appliquées : arrêt des bêtabloquants, arrêt des IEC et du sacubitril-valsartan, adaptation des doses des inhibiteurs du SRAA. Tous ces traitements ne vont pas être bénéfiques à ces patients qui ont un processus physiopathologique infiltratif responsable de l’hypertrophie cardiaque et de l’augmentation de l’épaisseur du myocarde, et qui va réduire la taille de la cavité ventriculaire, donc le volume d’éjection systolique. Or, on sait que le débit cardiaque est égal à la fréquence cardiaque fois le volume d’éjection systolique, et que les amyloses se caractérisent par un volume d’éjection systolique effondré, d’où la dangerosité de prescrire des bêtabloquants et la nécessité pour certains patients d’avoir des pacemakers.
En fonction du type, du stade de la maladie et du pronostic, proposition d’un traitement spécifique :
• Amylose TTR : le tafamidis est actuellement utilisé pour stabiliser la transthyrétine pathologique et ainsi empêcher son dépôt (traitement bien toléré, en prise orale). Ce traitement ne permet pas d’éliminer les dépôts déjà constitués, d’où l’intérêt de poser un diagnostic précocement. Il permet d’améliorer la survie après 15 mois de traitement.
• Amylose AL : un programme de chimiothérapie adapté.
L’acronyme CHAD-S-TOP rappelle la conduite à tenir thérapeutique chez les patients porteurs des amyloses :
• Prévenir les troubles de conduction cardiaque par des pacemakers.
• Prescrire des anticoagulants, l’amylose est une maladie très thrombotique et les AVC sont fréquents chez ces patients.
• Adapter les doses des diurétiques.
• Arrêter les médicaments recommandés dans l’insuffisance cardiaque.
À RETENIR
• L’amylose est une maladie systémique caractérisée par l’accumulation de fibrilles amyloïdes dans différents organes tels que le cœur, le rein, le foie, le système gastro-intestinal et nerveux, provoquant ainsi l’altération structurelle et fonctionnelle.
• Le diagnostic de l’amylose cardiaque repose sur le bilan biologique, l’ECG, l’échocardiographie, l’IRM cardiaque, la scintigraphie osseuse et la biopsie cardiaque.
• CHAD-S-TOP rappelle la conduite thérapeutique à tenir.
• Informations sur les amyloses disponibles sur le site www.reseau-amylose.org.
Bibliographie
1. Damy T. Amylose : une nouvelle cause d’insuffisance cardiaque chez le sujet âgé. Journée scientifique de Broca 2021.
2. Genet B, Courty B. Une insuffisance cardiaque réfractaire. Repères en gériatrie 2020 ; 23 : 95-102.
Carence martiale et insuffisance cardiaque chez le sujet âgé [1]
Le constat
Avec une prévalence de 10 % chez les sujets de 70 ans, et 20 % chez les sujets de 80 ans et plus, l’insuffisance cardiaque (IC) est une pathologie très fréquente dans la population âgée. Avec des conséquences lourdes sur la qualité de vie et le recours aux soins, elle est, en outre, responsable d’une mortalité de 50 % à 5 ans après le diagnostic.
Parmi les symptômes de l’IC, la dyspnée altère particulièrement la qualité de vie du patient âgé et interfère avec son maintien à domicile et la possibilité d’entrée dans un Ehpad. En effet, l’IC réduit l’autonomie fonctionnelle, la capacité de marcher et de faire de l’exercice, et est responsable de l’asthénie et de la fatigue matinale.
On retrouve ainsi pour cette population un recours aux soins non programmés, suivi par celui aux services de post-urgences, dont la gériatrie fait partie. En effet, 40 % des malades qui sont hospitalisés pour une IC sont réadmis dans les 12 mois qui suivent.
L’anémie
En cas d’insuffisance cardiaque, l’anémie (un taux d’hémoglobine inférieure à 130 g/l selon l’OMS) est un élément pronostic de déclin fonctionnel, de mortalité significativement supérieure (majoration de 13 % de mortalité avec baisse de l’hématocrite de 1 %) et de taux de ré-hospitalisation supérieur. Elle est fréquente dans la population âgée communautaire de plus de 80 ans, et est retrouvée chez 26 % des hommes et 20 % des femmes.
Si 30 % des anémies chez le sujet âgé sont des anémies carencielles (dont 50 % liées à une carence martiale), 30 % liées à des maladies chroniques (l’inflammation chronique, les cancers) et 30% à des maladies hématologiques, on notera cependant que les anémies physiologiques liées à l’âge n’existent pas.
Enfin, pour une anémie modérée avec un taux d’hémoglobine ≤ 115 g/l, la morbi-mortalité devient significativement supérieure chez les malades qui ont une IC.
Recommandations 2021 de l’European society of cardiology (ESC)
Au vu de ces données, et sachant que la carence martiale est une cause majeure d’anémie, les dernières recommandations 2021 de l’ESC indique que tout patient insuffisant cardiaque doit bénéficier d’un dépistage systématique d’une carence martiale.
Avant toute chose, il convient de distinguer la carence martiale absolue, définie par une ferritinémie < 30 mcg/l (< 100 mcg/l dans le domaine cardiologique) et la carence martiale fonctionnelle, définie par une ferritinémie comprise entre 100 et 200 mcg/l ainsi qu’un coefficient de saturation de la transferrine < 20 %.
Correction de la carence martiale
La correction de la carence martiale est proposée chez tout patient IC symptomatique avec une FEVG < 45 % afin de diminuer les symptômes et d’améliorer la capacité d’effort et la qualité de vie (recommandation de grade IIa, A), ou une FEVG < 50 % afin de réduire le risque d’hospitalisation pour IC (recommandation de grade IIa, B), (Tab. 1).
L’ESC recommande ainsi l’administration parentérale de carboxymaltose de fer (FERINJECT® ayant l’AMM en France pour l’IC). À noter que les autres spécialités n’ont pas été évaluées spécifiquement dans cette indication.
Dans tous les cas, la carence martiale devra être corrigée après avoir éliminé une cause inflammatoire, néoplasique ou hémorragique de l’anémie (Tab.1).
À RETENIR
• Anémie et insuffisance cardiaque sont des pathologies fréquentes et graves.
• L’anémie est un marqueur pronostique indépendant en cas d’insuffisance cardiaque dès le taux d’hémoglobine à 110 g/l.
• La carence martiale est une cause majeure de l’anémie.
• Le dépistage de la carence martiale est recommandé avec dosage de la ferritine et coefficient de saturation de la transferrine.
Bibliographie
1. Chassagne P. Carence martiale et insuffisance cardiaque chez le sujet âgé. Journée scientifique de Broca 2021.
Hémophilie acquise, quand y penser en gériatrie ? [1]
L’hémophilie acquise est une maladie hémorragique rare (1 cas/million/an) et grave, nécessitant une prise en charge rapide et adaptée afin de diminuer le risque de mortalité. Sa rareté retarde souvent son diagnostic, qui relève pourtant de l’urgence, engageant ainsi le pronostic du patient. Elle touche plus volontiers les patients âgés, les femmes enceintes et les post-partum.
Elle est due à l’apparition des auto-anticorps anti-facteur VIII ou anti-facteur IX neutralisant l’activité coagulante. Dans 50 % des cas, l’hémophilie acquise est idiopathique. Dans les autres cas, elle peut être associée à d’autres facteurs tels qu’un cancer, une maladie systémique (polyarthrite rhumatoïde) ou auto-immune (lupus érythémateux), ou encore une grossesse.
Manifestations
Elle se caractérise par un syndrome hémorragique d’apparition souvent spontanée ou à la suite d’un traumatisme mineur chez des patients sans antécédents personnels ou familiaux.
Dans 80 % des cas, on observe des saignements cutanéomuqueux (Fig. 1), mais d’autres complications hémorragiques, plus sévères, peuvent également survenir (des hématomes musculaires, des saignements digestifs, des saignements cérébraux). L’expression clinique diffère de celle observée au cours des hémophilies congénitales où le syndrome hémorragique se traduit surtout par des hémorragies musculaires et des hémarthroses.
On estime que 35 % des patients présentaient des manifestations hémorragiques pendant plus d’une semaine avant d’être diagnostiqués.
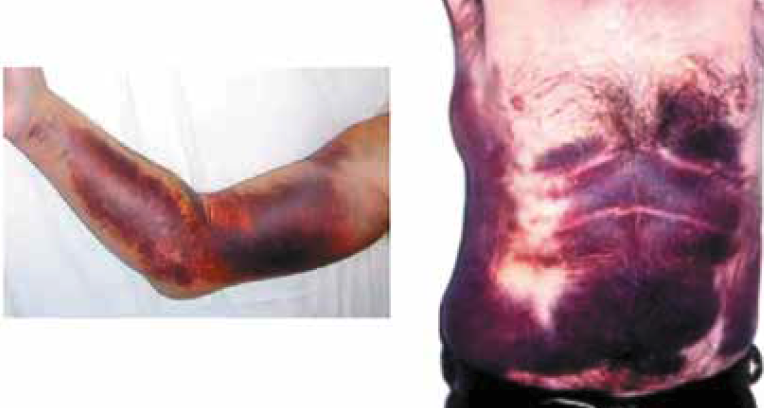
Figure 1 – Syndrome hémorragique cutanéomuqueux.
Diagnostic
Pour poser le diagnostic d’une hémophilie acquise (Fig. 2), un bilan de coagulation est nécessaire : un TCA allongé associé à un taux de prothrombine normal est l’élément-clé du diagnostic.
L’allongement du TCA est lié à la présence d’un anticoagulant circulant, mis en évidence par l’absence de correction du TCA par le mélange du plasma du malade avec un plasma de référence normal. Le diagnostic doit être confirmé par un dosage de facteur VIII inférieur à 30 % et un titre d’anticorps supérieur à 0,6 unité Bethesda (le test Bethesda démontre la spécificité de l’inhibiteur vis-à-vis du facteur VIII coagulant et permet de quantifier son titre).
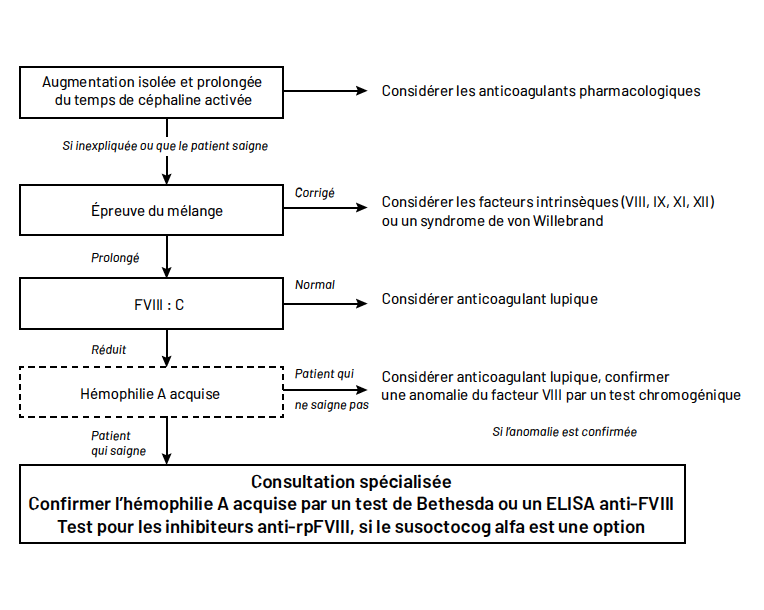
Figure 2 – Hémophilie acquise, la démarche diagnostique
Conclusion
L’hémophilie acquise est une urgence thérapeutique. Le patient doit être pris en charge en milieu spécialisé afin de contrôler le saignement et d’éradiquer l’inhibiteur. Dans les formes hémorragiques qui grèvent le pronostic vital et/ou fonctionnel, le recours à des facteurs anti-hémorragiques efficaces pourra être proposé : concentrés de complexes prothombiniques ou le facteur VII recombinant.
Par la suite, un traitement immunosuppresseur sera envisagé avec le recours à de la cortisone à 1 mg/ kg puis à dose décroissante sur 6 semaines dès l’augmentation de facteur VIII.
Dans certains cas peut se discuter le recours à des biothérapies, traitement ciblé visant à inactiver ou à bloquer une sous-population de lymphocytes : endoxan en PO à 2 mg/kg/jour sur 6 à 12 semaines ou rituximab à 375 mg/m2/semaine sur 4 semaines (absence d’AMM dans cette indication).
Encadré 1 – Hémophilie acquise, traitement par facteur VII recombinant.
- Dose utilisée : 90 microgrammes/kg toutes les 2 heures, injections rapprochées au début, puis espacer rapidement en fonction de l’efficacité
- Durée d’injection : 5 à 10 minutes par voie IV, sans dilution
- Durée moyenne de traitement : 6 jours (jusqu’au 36 jours)
- Complications : thrombose artérielle (< 8 %) avec décès (< 1 %)
- Surveillance : absence d’explorations biologiques
Encadré 2 – Hémophilie acquise, traitement par concentrés de complexes prothombiniques.
- Dose utilisée : 80 mg/kg toutes les 8 heures, à espacer rapidement en fonction de l’efficacité
- Durée d’injection : 30 à 45 minutes par voie IV, sans dilution
- Durée moyenne de traitement : 1 semaine en moyenne
- Complications : CIVD surtout si injection rapide, rares cas d’infarctus du myocarde et de thrombose veineuse
- Surveillance : absence d’explorations biologiques
À RETENIR
• L’hémophilie acquise se caractérise par l’apparition spontanée et inattendue d’un syndrome hémorragique, principalement chez des sujets sans antécédents.
• Il s’agit d’une urgence diagnostique et thérapeutique.
• Un bilan de coagulation doit être réalisé à la lecture des résultats. Si le TCA est allongé, il faut contacter un centre spécialisé.
Bibliographie
1. Frenzel L. Hémophilie acquise, quand y penser en gériatrie. Journée scientifique de Broca 2021.
Prise en charge de l’insuffisance cardiaque à fraction d’éjection préservée
L’insuffisance cardiaque à fraction d’éjection ventriculaire gauche (FEVG) préservée (HFpEF) est définie avec un niveau de la FEVG ≥ 50 %. La prévalence de cette pathologie augmente avec l’âge et fait de l’HFpEF la première cause d’hospitalisation dans les unités de court séjour gériatrique.
Selon les recommandations 2021 de l’European society of cardiology, le diagnostic d’HFpEF nécessite :
• des preuves objectives d’anomalies cardiaques structurelles ou fonctionnelles,
• des concentrations plasmatiques élevées de peptides natriurétiques compatibles avec la présence d’un dysfonctionnement diastolique du ventricule gauche (VG)
• et une augmentation des pressions de remplissage du VG.
Un test d’effort diastolique est recommandé lorsque ces marqueurs sont équivoques.
Prise en charge
Jusque récemment, aucun traitement n’a démontré la réduction de la mortalité et la morbidité chez les patients atteints d’HFpEF (Tab.1).
Cependant, compte tenu :
• du risque associé élevé d’événements cardiovasculaires et non cardiovasculaires (faisant d’elle une des principales causes d’hospitalisation et de perte d’autonomie),
• de l’augmentation de la prévalence de la fragilité et donc de mortalité,
• et de la prévalence de l’insuffisance cardiaque (IC) augmentant avec l’âge – avec une mortalité à un an étant de 35 % chez les IC âgés de 80 à 89 ans, et de 50 % après 90 ans,
le consensus des experts [2] a proposé en 2021 la prise en charge de de l’insuffisance cardiaque (IC) chez les sujets très âgés comme présenté dans la figure 1. L’objectif du traitement de l’insuffisance cardiaque après 80 ans est de réduire les symptômes, la mortalité et les hospitalisations, mais aussi d’améliorer la qualité de vie. En l’absence d’études spécifiques réalisées chez des sujets très âgés, la plupart des recommandations sont extrapolées à partir de données provenant de populations plus jeunes.
NB : Chez les personnes âgées, l’existence d’une fragilité doit faire réaliser une évaluation gériatrique multidimensionnelle afin de prendre en charge les syndromes gériatriques comme les troubles cognitifs, les chutes, la dénutrition, la dépression, la iatrogénie, la perte d’autonomie et l’isolement social.
Globalement, les études épidémiologiques indiquent une prescription insuffisante des médicaments recommandés dans l’insuffisance cardiaque, alors que les bénéfices des traitements sont pourtant observés indépendamment de l’âge. Cette sous-prescription peut être liée aux comorbidités et à la peur des effets secondaires ou à l’absence de recommandations spécifiques dans le cadre de l’IC à fraction d’éjection préservée, pourtant fréquente dans cette population. Ainsi, le rapport bénéfices/risques des médicaments de l’insuffisance cardiaque doit être évalué régulièrement au cours du suivi. Enfin, la prise en compte du pronostic de la maladie en fonction des facteurs prédictifs de mortalité peut aider à mieux définir le plan de soins et à promouvoir des soins palliatifs si besoin.
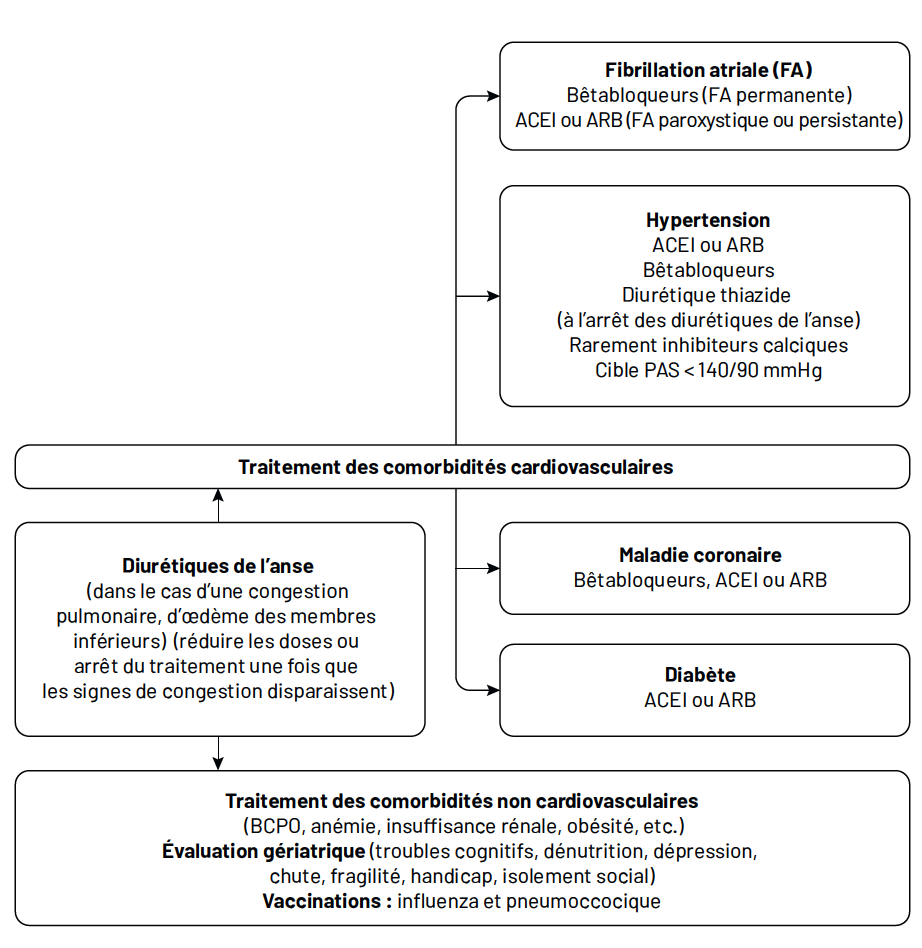
Figure 1 – Prise en charge de de l’IC chez les sujets très âgés.
Zoom sur les inhibiteurs de SGLT2
Les inhibiteurs de SGLT2 (iSGLT2) ont prouvé leur efficacité dans la réduction de la mortalité cardiovasculaire et d’hospitalisations en cas d’IC à FEVG altérée [3]. À ce titre, l’étude EMPEROR-Preserved avait pour objectif d’évaluer les effets de l’empagliflozine dans l’HFpEF.
Ainsi, après un suivi de 26 mois, le traitement par empagliflozine a montré une réduction significative de la survenue des décès cardiovasculaires et des hospitalisations pour insuffisance cardiaque, sans effets indésirables notables. Il a fallu 31 patients pour observer l’évitement d’un décès cardiovasculaire ou d’une hospitalisation pour insuffisance cardiaque. Les résultats encourageants de cette étude indiqueraient ainsi que l’empagliflozine serait le premier traitement ayant démontré son efficacité dans l’HFpEF.
Étude EMPEROR-Preserved
Méthodologie
Un essai international, EMPEROR-Preserved, a été mené dans 622 centres et 23 pays [4]. Cette étude a inclus 5 988 patients insuffisants cardiaques symptomatiques (Classe NYHA 2 à 4) avec fraction d’éjection préservée (FEVG > 40 %, moyenne à 54 %) ; les deux-tiers des patients avaient une FEVG > 50 %.
Parmi ces patients, âgés en moyenne de 72 ans (45 % de femmes), la moitié avait des antécédents de diabète de type 2. Ils ont été randomisés pour recevoir de l’empagliflozine (10 mg/j) ou un placebo en plus de leur traitement standard.
Le critère de jugement principal était le composite de la mortalité cardiovasculaire et des hospitalisations pour IC. Les critères secondaires étaient les hospitalisations pour IC et le taux de déclin du débit de filtration glomérulaire (DFG).
Résultats
Après un suivi médian de 26 mois, les résultats ont montré que le critère principal d’évaluation (mortalité cardiovasculaire et hospitalisation pour insuffisance cardiaque) est survenu chez 415 des 2 997 patients (13,8 %) ayant reçu l’empagliflozine, et chez 511 des 2 991 patients (17,1 %) du groupe placebo. Soit 21 % d’événements en moins chez les patients sous iSGLT2 (HR = 0,79 ; IC à 95 %, [0,69–0,90], p = 0,0003) (Fig. 2).
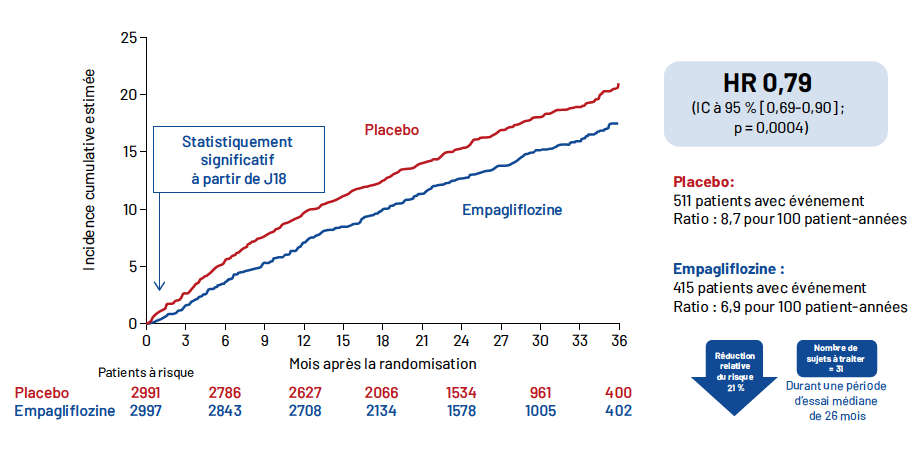
Figure 2 – Effet de l’empagliflozine sur le critère de jugement principal.
Le bénéfice de l’empagliflozine a été observé dans tous les sous-groupes (âge, IMC, patients avec ou sans diabète) et pour les groupes des patients ayant une FEVG comprise entre 40 et 50 %, et comprise entre 50 et 60 %. Cependant, l’effet était neutre pour les FEVG
> 60 %. Cette différence est principalement due à une diminution du nombre d’hospitalisations pour IC inférieure dans le groupe traitement par empagliflozine (HR = 0,73 ; p < 0,001).
Le déclin du DFG était aussi plus lent dans le groupe traitement (-1,25 vs -2,62 ml/min/1,73m2/an ; p < 0,0001) (Fig. 3). Sous empagliflozine, il apparaît d’abord une dégradation soudaine et transitoire de la fonction rénale, qui diminue ensuite lentement.
Les effets indésirables sous empagliflozine n’étaient pas significatifs (47,9 % vs 51,6 % sous placebo), même si les infections génitales et urinaires non compliquées, ainsi que les hypotensions ont été plus fréquentes sous empagliflozine.
Il n’y a pas de différence entre les groupes traitement et placebo pour les fractures osseuses (4,5 % vs 4,2 %) ou les acidocétoses (0,1% vs 0,2%).
Toutefois, les résultats montrent l’absence d’amélioration significative sur la mortalité cardiovasculaire, la mortalité globale, la qualité de vie et le nombre total d’hospitalisations (toutes causes) dans EMPEROR-Preserved.
Le mécanisme physiopathologique des gliflozines sur l’amélioration de la fonction cardiaque n’est pas encore bien élucidé. Les hypothèses évoquées sont la baisse de la volémie consécutive à l’effet diurétique de ces médicaments, une amélioration du métabolisme énergétique et un meilleur équilibre de l’homéostasie.
Malgré cela, l’empagliflozine pourrait représenter la première opportunité réelle de traitement des IC à FEVG préservée, et marque ainsi un tournant très intéressant dans la prise en charge pluridisciplinaire des patients IC et patients polypathologiques.

Figure 3 – Effets de l’empagliflozine sur le critère de jugement principal et sur les critères de jugement secondaires.
L’auteure déclare ne pas avoir de lien d’intérêt.
À RETENIR
• L’IC à FEVG préservée est la forme d’IC la plus fréquente en gériatrie.
• Selon les dernières recommandations de l’ESC 2021, le traitement consiste en l’administration des diurétiques de l’anse en phase congestive et prise en charge des comorbidités (HTA, FA, BPCO…).
• L’étude EMPEROR-Preserved est une étude révolutionnaire : l’empagliflozine est le premier traitement ayant démontré son efficacité dans l’HFpEF à dose de 10 mg/j.
Bibliographie
1. Hanon O. Prise en charge de l’insuffisance cardiaque à fraction d’éjection préservée. Journée scientifique de Broca 2021.
2. Hanon O, Belmin J, Benetos A et al. Consensus of experts from the French Society of Geriatrics and Gerontology on the management of heart failure in very old subjects. Arch Cardiovasc Dis 2021 ; 114 : 246-59.
3. Packer M, Anker SD, Butler J et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. New Engl J Med 2020 ; 383 : 1413-24.
4. Anker SD, Butler J, Filippatos G et al. Empagliflozin in Heart Failure with a Preserved Ejection Fraction. New Engl J Med 2021 ; 385 : 1451-61.